Vacuna COVID-19 de Johnson & Johnson recibe luz verde para reanudar su distribución
“Estamos seguros de que esta vacuna sigue cumpliendo con nuestros estándares de seguridad, eficacia y calidad”, dijo la comisionada interina de la FDA, Janet Woodcock.
Únete al canal de Whatsapp de El Popular- Confirmado | Exigen el retiro urgente de este pescado de los supermercados por ser un riesgo mortal para la población
- ALARMA en Walmart: ICE se burló y arrestó a padre de familia que huyó de la guerra de Ucrania hacia EE.UU.
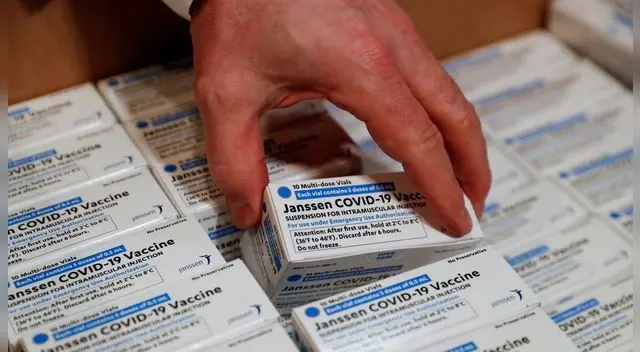
Los reguladores federales de Estados Unidos autorizaron la reanudación de la distribución de la vacuna contra el coronavirus de Johnson & Johnson, el viernes 23 de abril, tras una revisión de un panel de expertos que determinó que cumple con los estándares de seguridad.
La Administración de Alimentos y Medicamentos (FDA) y los Centros para el Control y la Prevención de Enfermedades (CDC) levantaron la pausa de 10 días, tras la aparición de extraños casos de coágulos sanguíneos graves.
El panel de CDC recomendó la inclusión de un lenguaje que advirtiera al público del riesgo de coágulos de sangre al recibir la vacuna de dosis única.
"Hemos llegado a la conclusión de que los beneficios conocidos y potenciales de la vacuna Janssen COVID-19 superan sus riesgos conocidos y potenciales en personas de 18 años o más", dijo la comisionada interina de la FDA, Janet Woodcock, en un comunicado.
“Estamos seguros de que esta vacuna (Johnson & Johnson) sigue cumpliendo con nuestros estándares de seguridad, eficacia y calidad”, agregó.
Los funcionarios de salud detuvieron el lanzamiento de la vacuna Johnson & Johnson, el pasado 13 de abril en respuesta a seis casos reportados de trombosis con síndrome de trombocitopenia (TTS).
En ese momento, la FDA dijo que había recomendado una pausa y una revisión de seguridad posterior por precaución.
La FDA y los CDC dijeron que han identificado un total de 15 casos entre casi ocho millones de receptores, todos los cuales ocurrieron en mujeres de entre 18 y 59 años. Tres de las mujeres murieron y siete permanecen hospitalizadas.
Las autoridades dijeron que los síntomas asociados con los coágulos de sangre aparecieron entre seis y 15 días después de la vacunación.
"En este momento, los datos disponibles sugieren que la posibilidad de que ocurra TTS es muy baja, pero la FDA y los CDC permanecerán atentos para continuar investigando este riesgo", dijeron las agencias en un comunicado de prensa.
Los reguladores de Europa tomaron una decisión similar a principios de esta semana y permitieron que se reanudara el lanzamiento de la vacuna Johnson & Johnson.
Revisa todas las noticias escritas por el staff de redactores de El Popular.












